下半年《物理化学实验》-生态环境系
-
此课程由化学与材料科学学院负责,面向生态环境系环工、环科本科生。
-
教学地点:五四路校区化学楼402实验室
-
主要教材:《基础化学实验4——物性参数与测定》 马志广、庞秀言主编 化学工业出版社 2016年
-
下载百度网盘,包含大纲、教案&预做实验、绘图代码、电导率仪手册、学生实验报告等。
电导法测定弱电解质的电离平衡常数
实验思路
-
本实验需要测量乙酸的电离平衡常数,而电离平衡常数与浓度有关(见P65,式(1))。因涉及到弱电解质乙酸,所以浓度需要考虑电离度α。
-
采用电导法测定电离度α(见P66,式(6))。
-
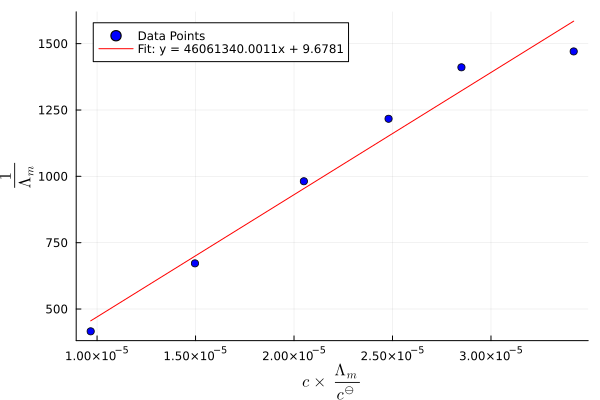
依据式(7)画图,先求得截距,再根据斜率求出电离平衡常数。
数据处理
-
学习三线表的标准格式,实验报告、论文等表格应遵循三线表格式要求。
-
表格易错处
表2 电导率测定结果
-
κ(HAc)=κ(溶液)-κ(水)
-
κ(水)一般小于10 µS·cm-1,即10*10-4 S·m-1
-
求解1/Λm(HAc)时,考虑Λm=κ/c。
-
求解cΛm(HAc)/c⊖时,考虑c⊖=1000 mol/m3。
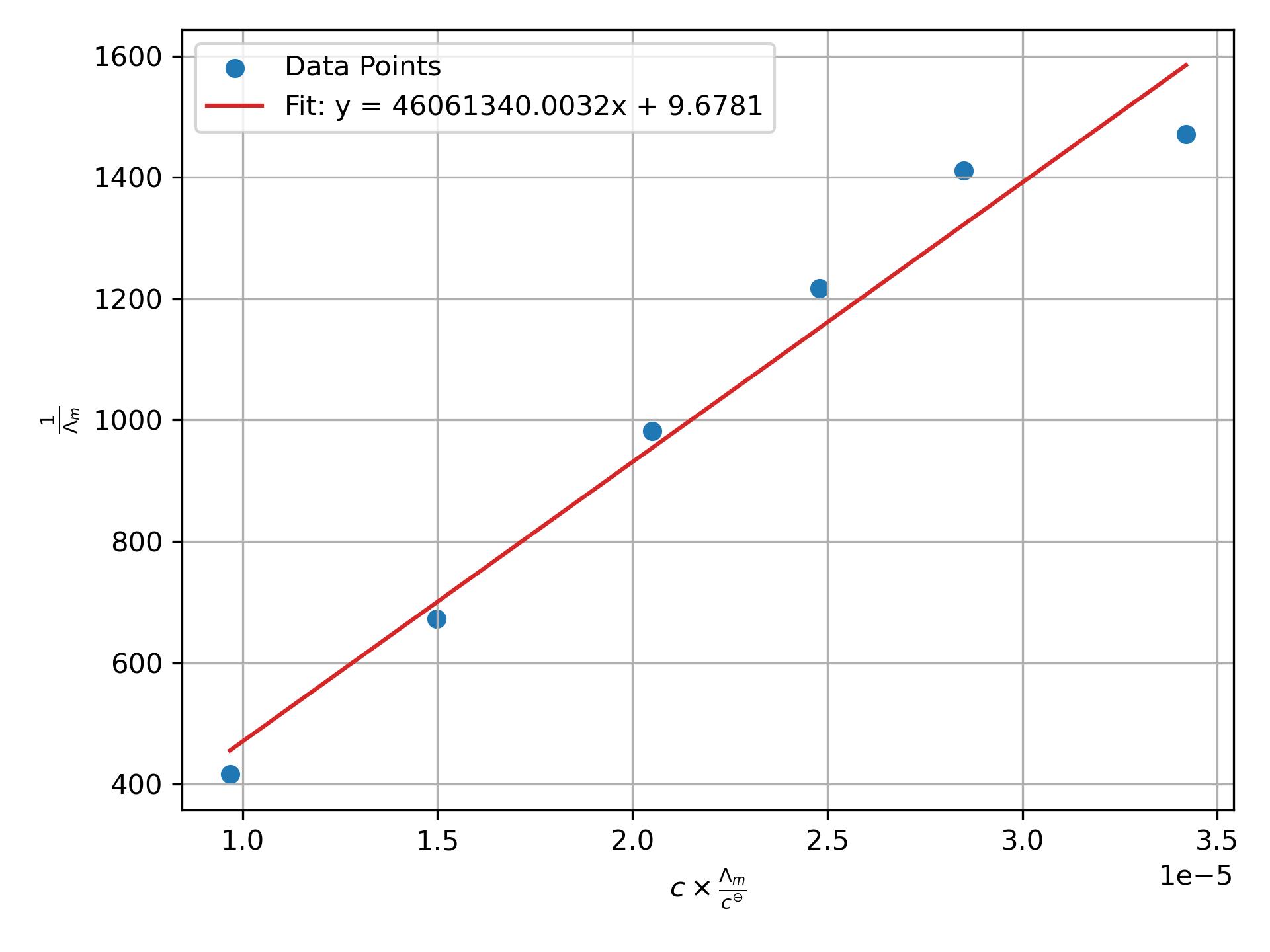
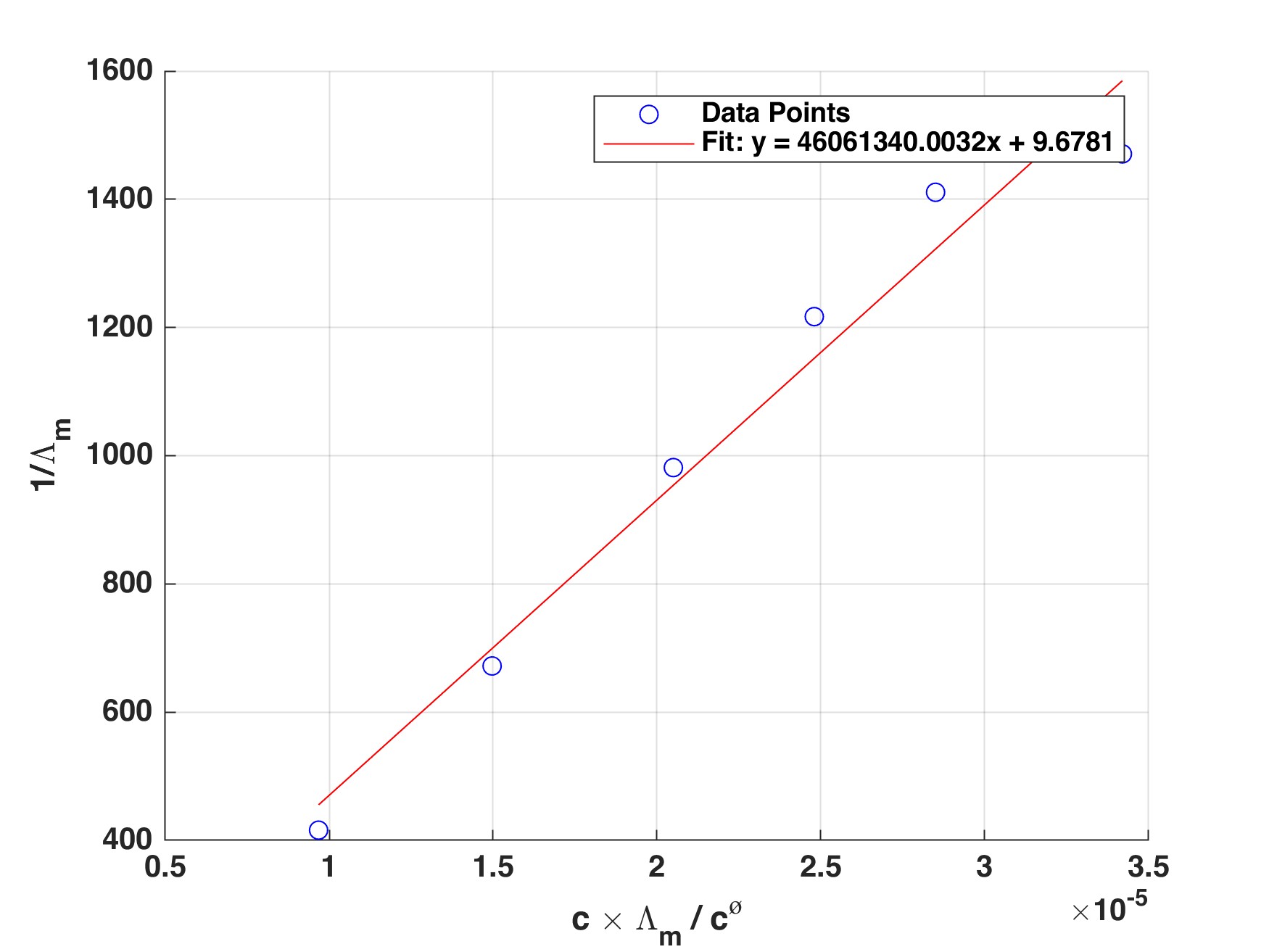
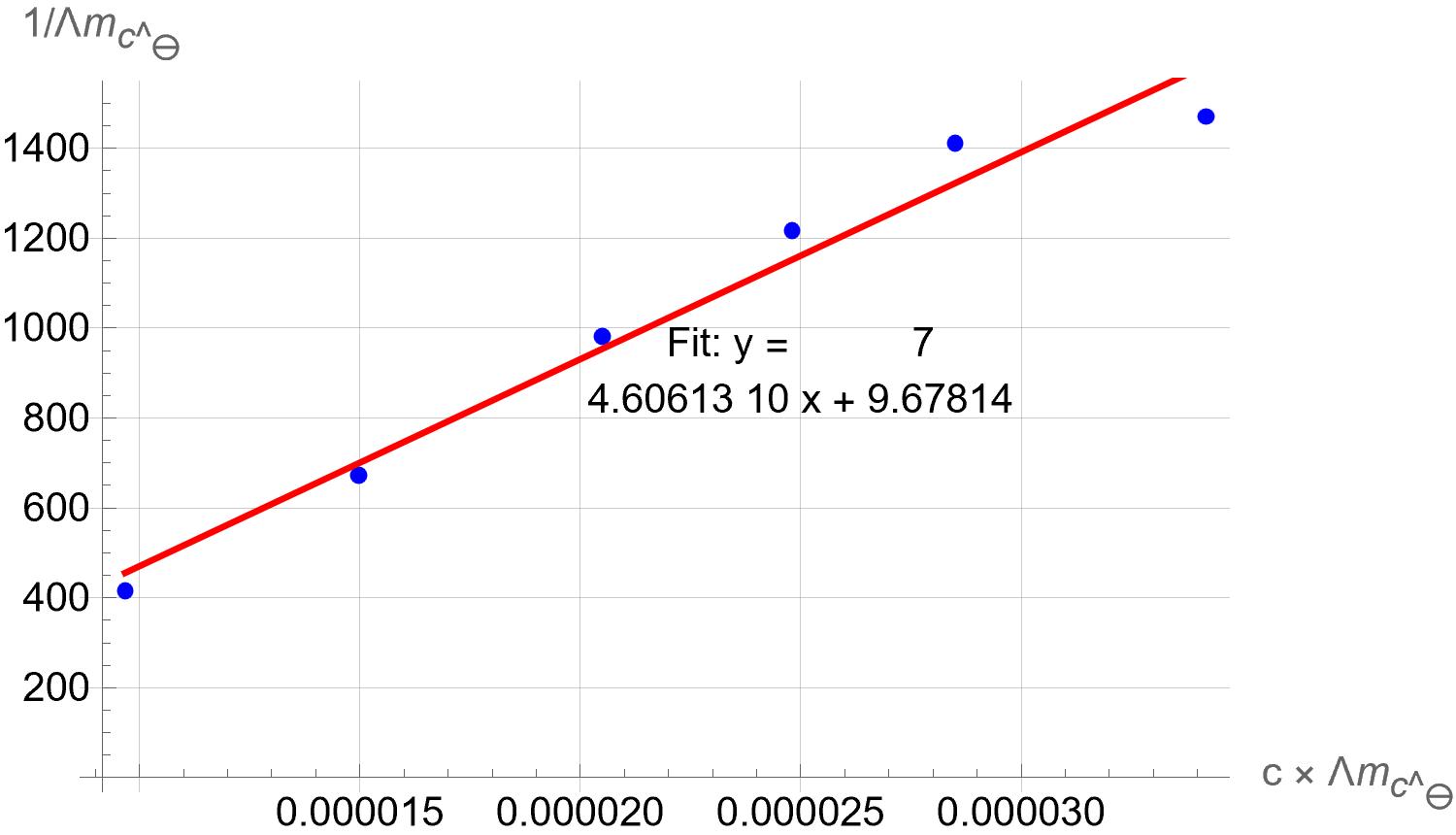
Origin作图
- λm-1为y,cλm/c⊖为x,填写
Book1。
- 选中作图所需的数据,点击
绘图-散点图。
- 选中
分析-拟合-线性拟合,获得线性拟合方程。
- 双击图中对应的位置,修改图的坐标轴等。
-
Origin出图显示
demo是因为破解不完全所致。 -
x轴、y轴单位别遗漏,此实验的图都有这个bug。
Python作图
- 代码:
|
|
- 作图:
Matlab作图
- 代码:
|
|
- 作图:
Mathematica作图
- 代码:
|
|
- 作图:
Julia作图
- 代码:
|
|
- 作图:
蔗糖转化反应速率常数的测定
实验思路
-
蔗糖水解反应是一级反应,其反应速率常数与浓度有关;而浓度的实时测量需要与之成正比的旋光度α进行替换。
-
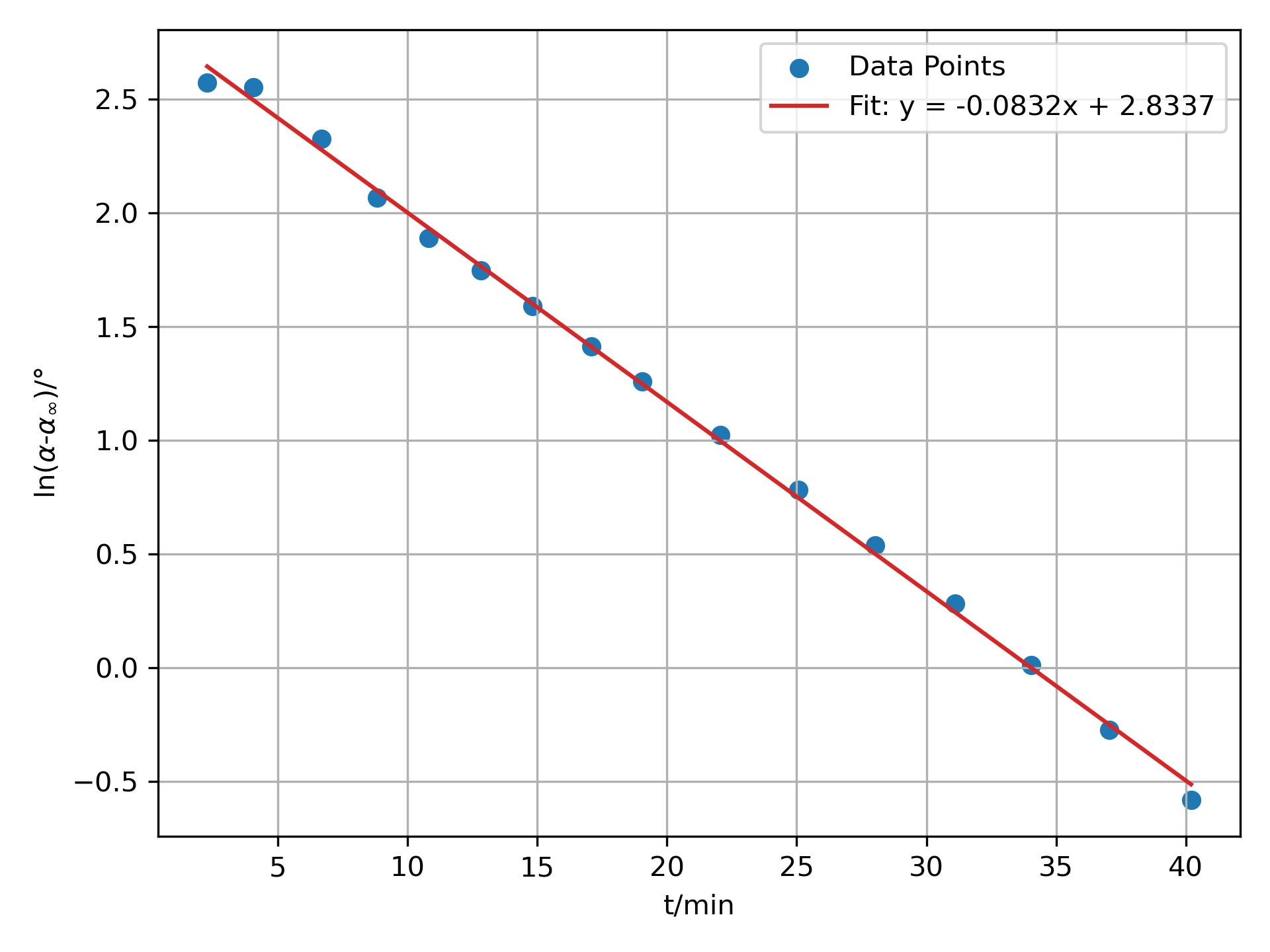
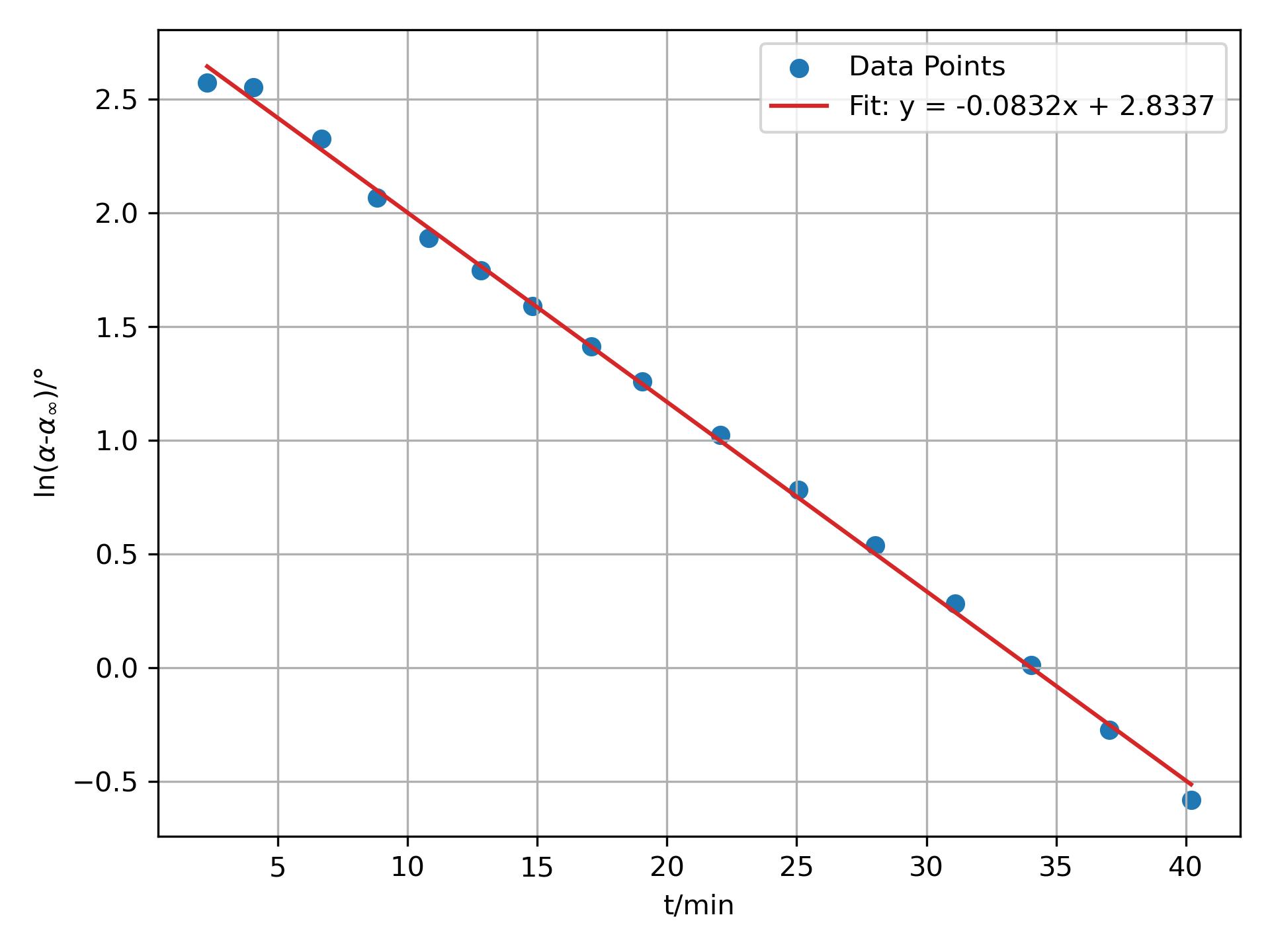
旋光度α的测量需要旋光仪。根据P51 式(7),需要测得一系列不同t时刻下的α和反应完全的α∞,代入式(7)作图,由斜率可得反应速率常数k。
-
根据上一步的k,再加上一级反应的特点(见P50 式(2))可知半衰期。
对于简单级数反应的半衰期:
-
零级反应的半衰期与反应的起始浓度成正比
-
一级反应的半衰期与反应的起始浓度无关
-
二级反应的半衰期与反应的起始浓度成反比
数据处理
-
根据P52
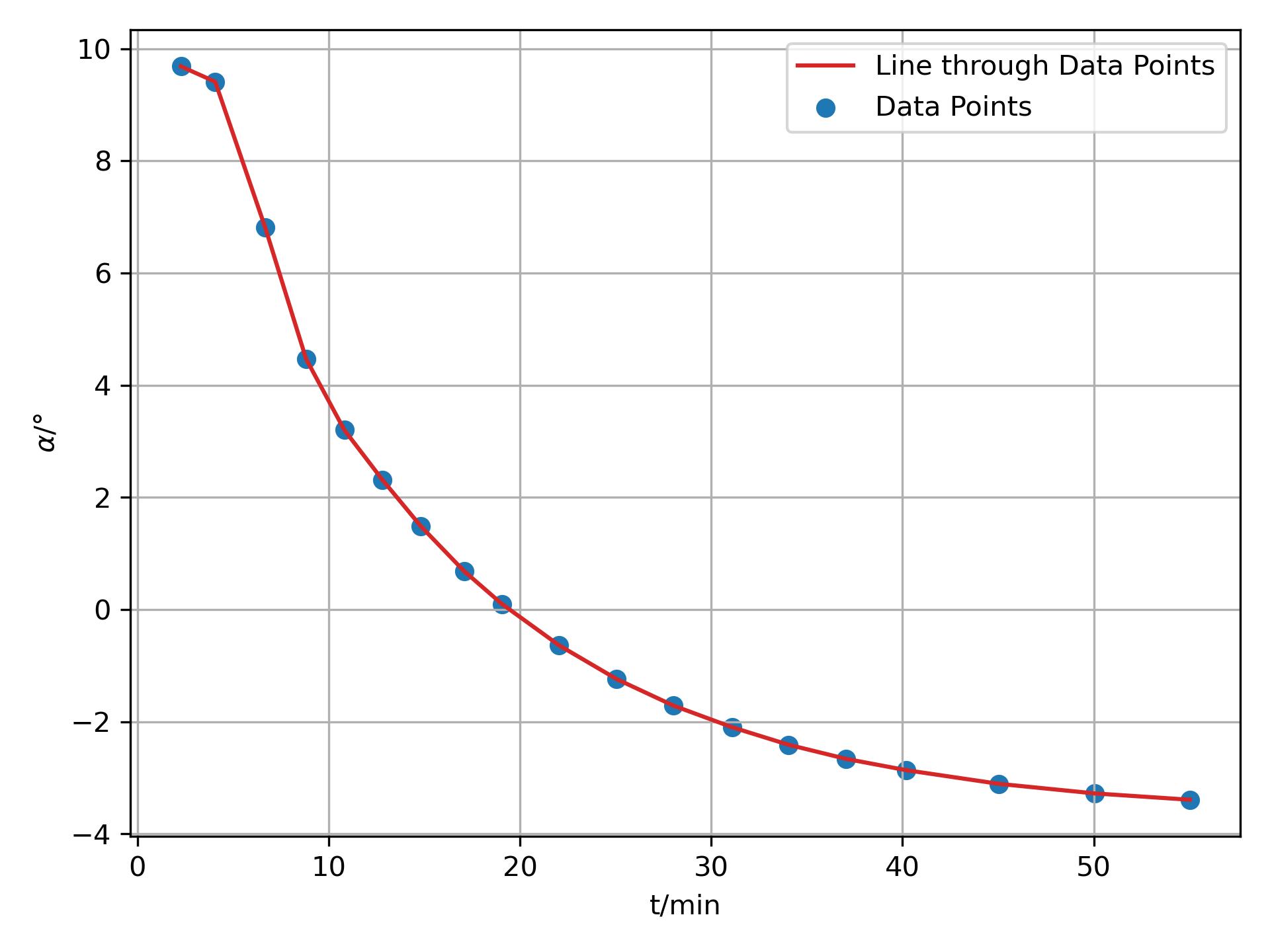
2. 作α-t图和4. 作ln[(α-α∞)/°]-t作图,因此,实验报告是两个图,不要遗漏! -
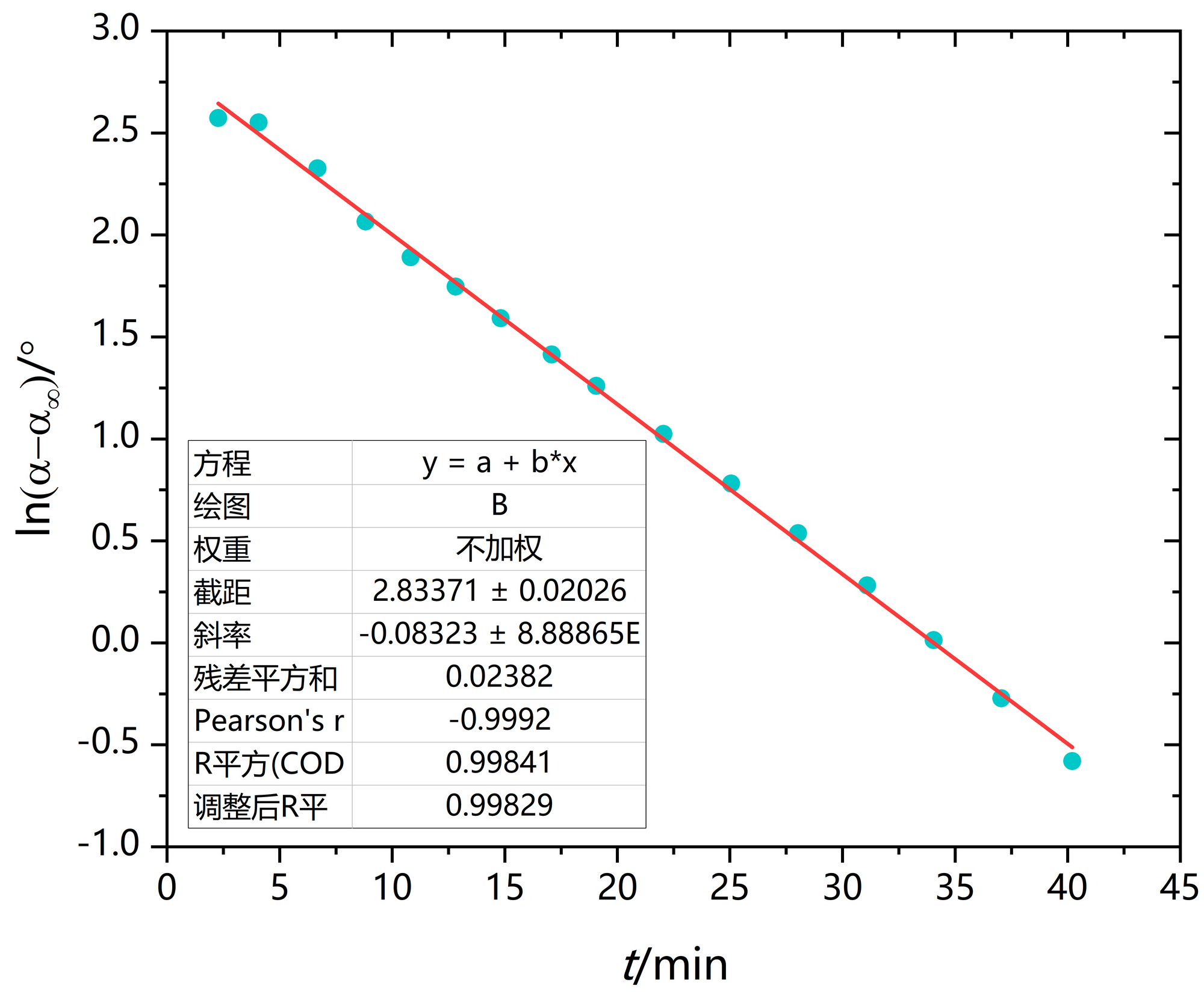
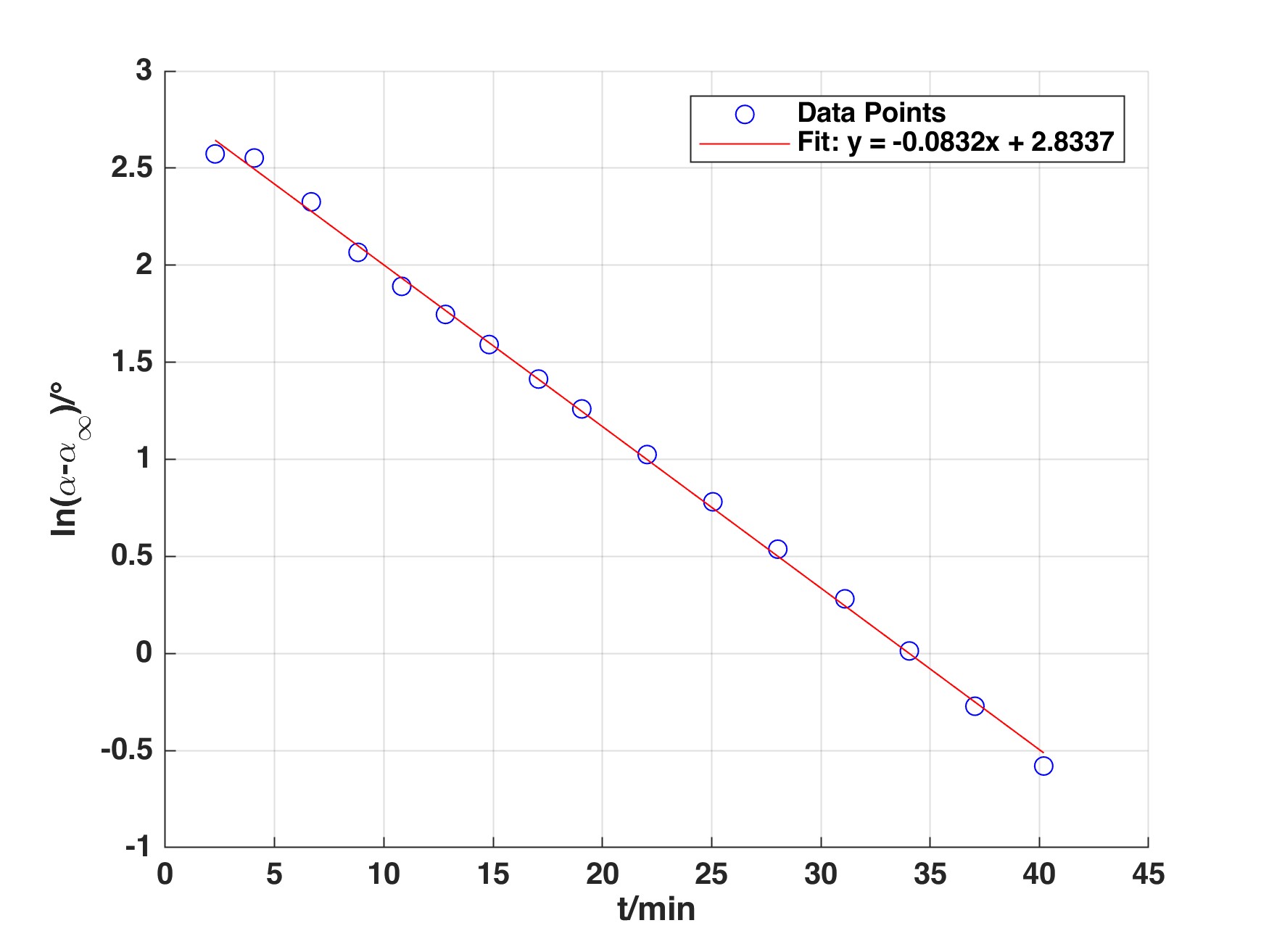
4.作ln[(α-α∞)/°]-t作图时,用y = kx + b线性方程拟合。
-
蔗糖水解反应是一级反应,速率常数k的单位是min-1。
-
半衰期是min。
-
实验报告上这两个单位不要遗漏!
Origin作图
- 虚线不是必须,只是方便显示在19~20 min,旋光度由正变负。
Python作图
2. 作α-t图代码:
|
|
2. 作α-t图作图:
4. 作ln[(α-α∞)/°]-t代码:
|
|
4. 作ln[(α-α∞)/°]-t作图:
Python+Keras作图
4. 作ln[(α-α∞)/°]-t代码:
|
|
4. 作ln[(α-α∞)/°]-t作图:
Matlab作图
2. 作α-t图代码:
|
|
2. 作α-t图作图:
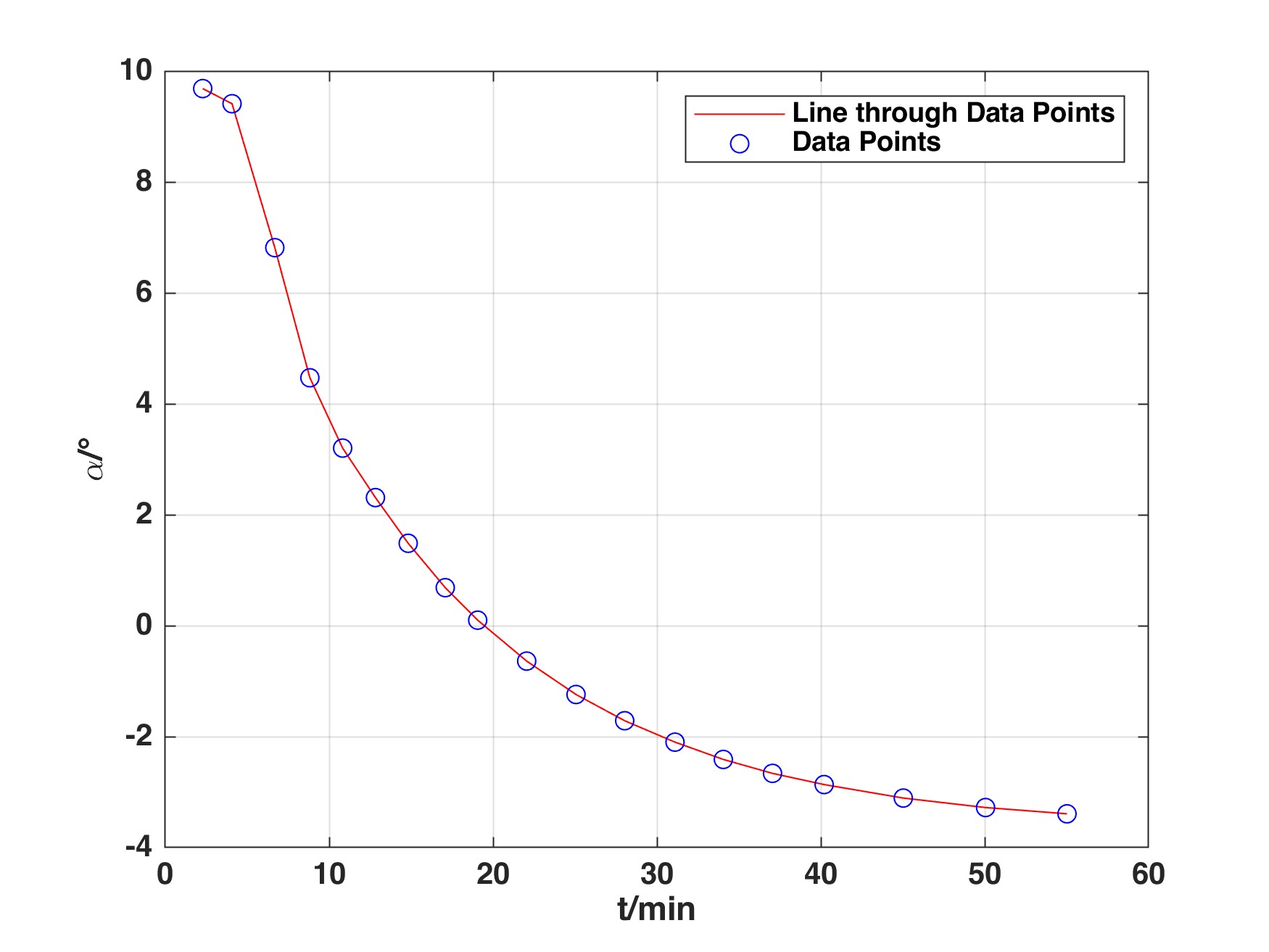
4. 作ln[(α-α∞)/°]-t代码:
|
|
4. 作ln[(α-α∞)/°]-t作图:
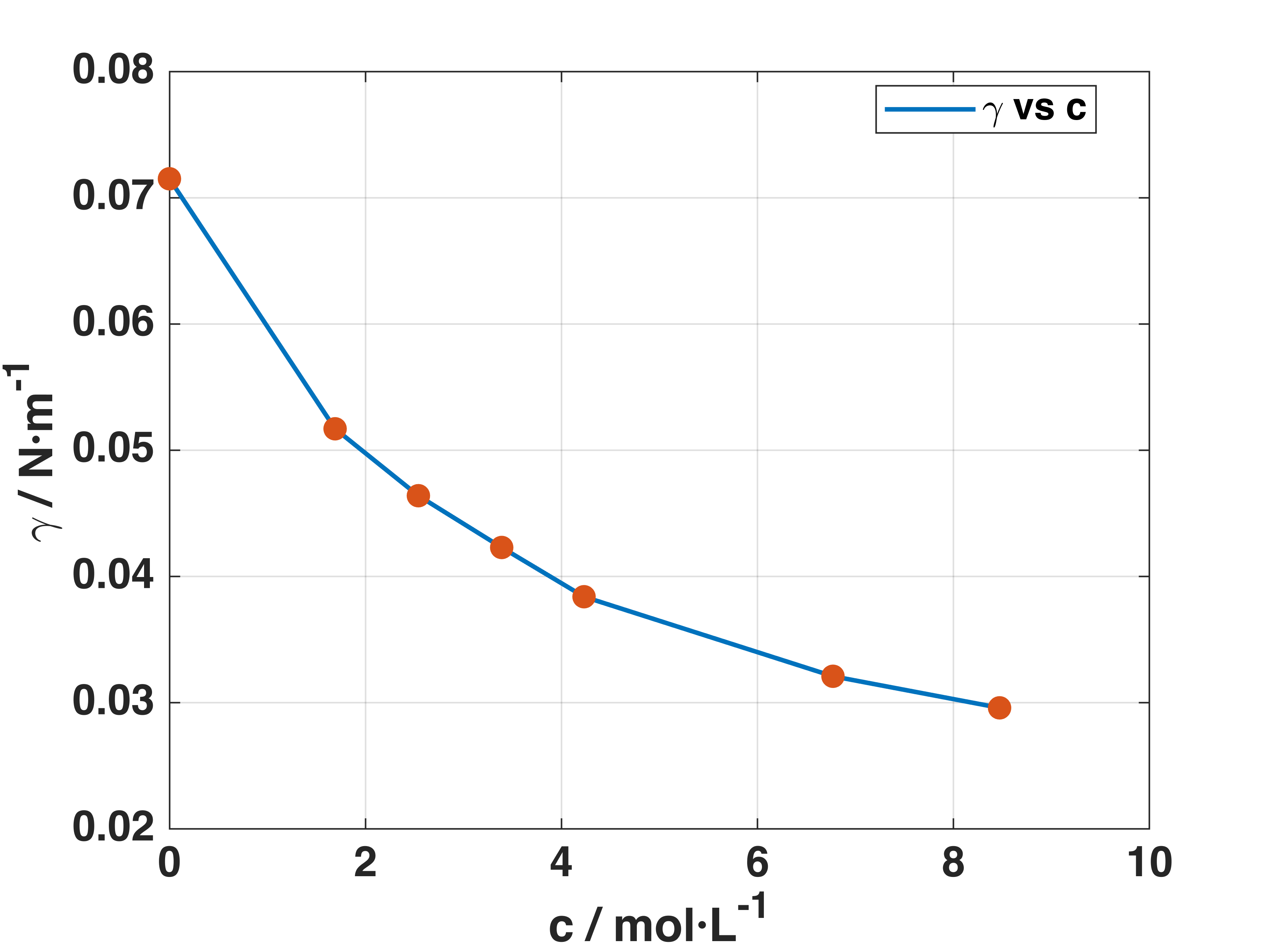
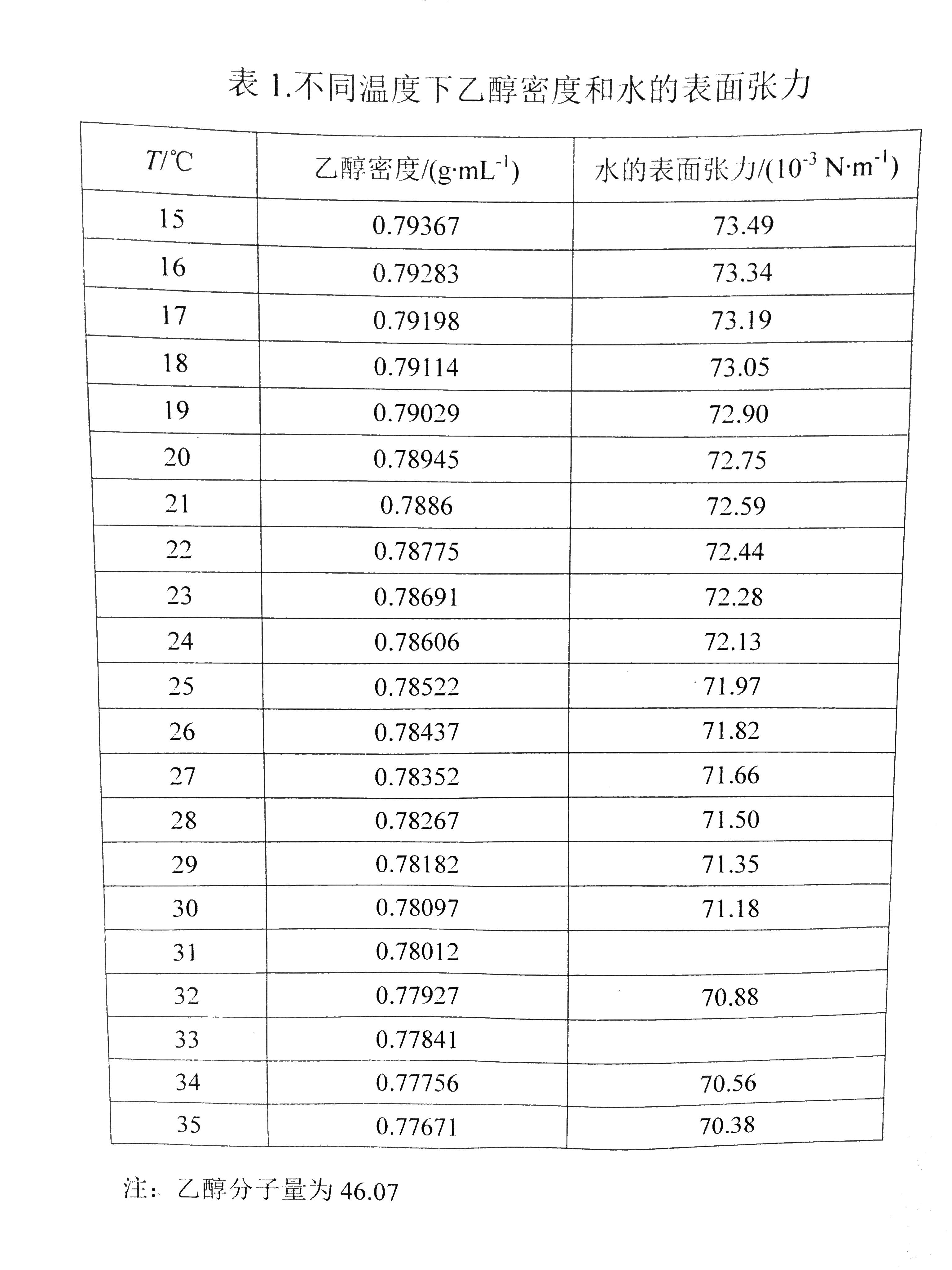
溶液表面张力的测定
Python作图
- 代码:
|
|
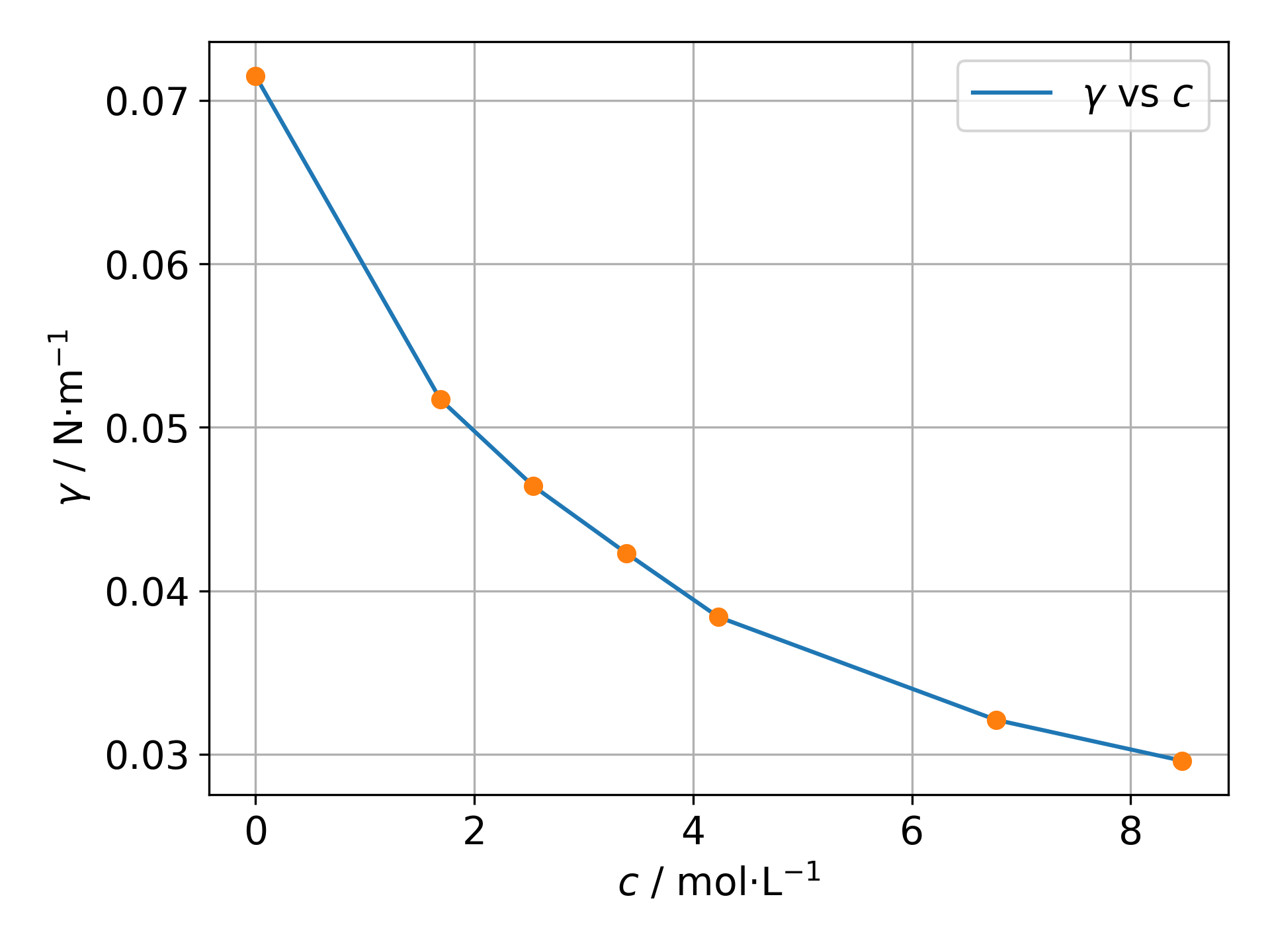
- 作图:
Matlab作图
- 代码:
|
|
- 作图: